Rendez-vous d’information patients, aidants et donneurs du 07 mars 2023 de la SFGM-TC
Le microbiote intestinal au cœur de notre santé
Présentation de Dr Julien SCANZI, hépato-gastroentérologue aux CH de Tiers et CHU d’Estaing
L’intestin n’est pas juste un tube ou un outil de digestion, il héberge un véritable écosystème : notre microbiote intestinal.
Un microbiote comprend l’ensemble des organismes invisibles à l’œil nu vivant au sein d’un écosystème. On peut y retrouver notamment des bactéries, mais aussi des virus, des levures, des champignons, des archées, des parasites… Notre corps en abrite à chaque interface avec son environnement : le microbiote intestinal, cutané, buccal, vaginal ou pulmonaire.
Le microbiote intestinal est de loin le plus riche, surtout dans le côlon, et le mieux étudié car il a un lien étroit avec notre santé. On estime d’ailleurs qu’un gramme de selles contient 100 milliards de bactéries et que la quantité de l’ADN bactérien est 100 à 150 fois plus importante que celle de l’ADN humain. Le microbiote intestinal est propre à chaque individu.
La recherche dans ce domaine est très récente puisqu’elle a commencé il y a seulement quelques décennies.
Évolution du microbiote intestinal au cours du temps
Le tube digestif étant stérile in utero, l’acquisition d’un microbiote intestinal se fait à la naissance de façon différente selon l’origine ethnique et géographique, le mode d’accouchement (césarienne ou voie basse), le microbiote maternel et l’environnement immédiat du bébé.
La composition de notre microbiote évolue tout au long de notre vie en fonction de notre environnement, de l’alimentation et de la prise de certains médicaments comme les antibiotiques. Elle évolue ensuite beaucoup moins après l’âge de 3-5 ans, en fonction de facteurs endogènes (vieillissement, stress, maladie, etc.) mais surtout exogènes (alimentation, médication, pollution, etc.).
Un deuxième cerveau ?
L’intestin à un système nerveux autonome : le système nerveux entérique composé de plus de 200 millions de neurones dont 80% envoient leurs informations vers le cerveau. Cet axe de communication neuronale est appelé l’axe cerveau-intestin. La recherche a montré son implication dans de nombreuses pathologies, par exemple l’anxiété et la dépression, via la synthèse et la régulation d’hormones comme la sérotonine.
Principales fonctions des bactéries intestinales
- Digestion des fibres par fermentation.
- Assimilation des médicaments. La réponse de l’organisme à certains traitements (ex : traitements anticancéreux comme la chimiothérapie ou l’immunothérapie) est dépendante de la composition du microbiote intestinal de chaque individu.
- Maturation et stimulation du système immunitaire. Un microbiote intestinal altéré ou dysfonctionnel aura un retentissement sur le système immunitaire, et inversement.
- Production de métabolites : vitamines, acides gras à chaînes courtes, sérotonine, cytokines…
- Effet barrière : protection contre les pathogènes de l’environnement
La symbiose, un équilibre fragile
Symbiose (du grec : synbiosis “vie ensemble”) : association étroite de deux ou plusieurs organismes différents mutuellement bénéfique, voire indispensable à leur survie.
Nous vivons en symbiose avec notre microbiote intestinal. Si nous leur apportons de quoi proliférer comme une alimentation riche en fibre ou une activité physique régulière, nous maintenons leur biodiversité nécessaire à une bonne santé physique et mentale. À l’inverse, de nombreux facteurs peuvent perturber le microbiote intestinal et ainsi mettre à mal cet état de symbiose et favoriser le développement de maladies chroniques : une alimentation transformée avec des produits cultivés avec des pesticides, ou contenant des additifs, la pollution de l’air et de l’eau, le stress, la sédentarité, ainsi que certains médicaments (antibiotiques, antiacides, etc.).
Dysbiose et résilience
La dysbiose est un déséquilibre de l’écosystème micro-bactérien. Elle se traduit par une perte de la richesse et de la diversité du microbiote qui altère la symbiose hôte-microbiote.
Cette altération peut notamment être liée :
- au vieillissement;
- au mode de vie : alimentation, sédentarité;
- aux xénobiotiques : médicaments (surtout les antibiotiques), additifs alimentaires, pollution.
Malgré tout, le microbiote est résilient, c’est-à-dire qu’il est capable d’absorber certains chocs et certains changements pour revenir à un état d’équilibre symbiotique. Cette capacité de résilience est malheureusement limitée si les agressions sont trop importantes ou répétées dans le temps. Il va alors s’altérer durablement et se stabiliser dans un état de dysbiose. Ce risque est d’autant plus important quand le microbiote est en construction, c’est-à-dire dans la petite enfance, avant l’âge de 2 à 3 ans.
Vers une extinction de notre faune intestinale ?
Plusieurs études se sont intéressées à la composition de plusieurs peuples, parmi lesquels certains ayant un mode de vie de chasseurs-cueilleurs se rapprochant de celui de nos ancêtres. Ces peuples possèdent un microbiote intestinal bien plus riche et diversifié en micro-organismes que les populations occidentales (en l’occurrence les États-uniens). L’hypothèse principale est que notre microbiote s’appauvrit au fil des décennies.
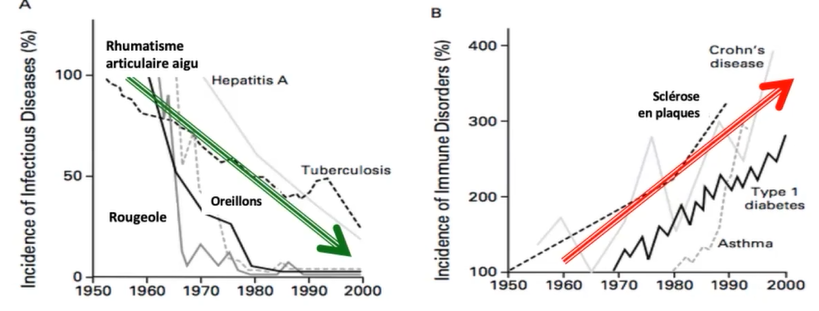
C’est d’ailleurs au cours de ces dernières décennies qu’on a pu observer une baisse de l’incidence des maladies infectieuses, notamment grâce aux avancées de l’hygiène, au perfectionnement des traitements antibiotiques et à la vaccination. A l’inverse, on remarque une hausse significative des maladies liées à un dysfonctionnement du système immunitaire et des maladies métaboliques. Une partie de la recherche soutient une hypothèse hygiéniste affirmant que l’explosion de ce type de maladie était due à un excès d’hygiène et à l’utilisation démesurée des antibiothérapies.
Une autre hypothèse est l’hypothèse microbienne certifiant une corrélation entre la hausse de l’incidence des maladies liées au système immunitaire et l’appauvrissement de notre microbiote intestinal.
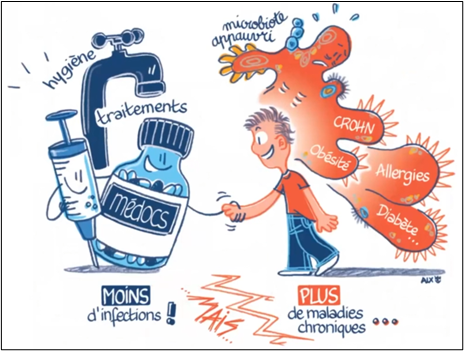
Ainsi, l’excès d’hygiène (aseptisation, surconsommation d’antibiotiques, de pesticides) et une alimentation de plus en plus pauvre en fibres sont des facteurs propices à un appauvrissement du microbiote intestinal qui serait lui-même – au moins en partie – à l’origine de la forte hausse des maladies métaboliques et dysimmunitaires de ces dernières décennies.
©Alice Varoquaux
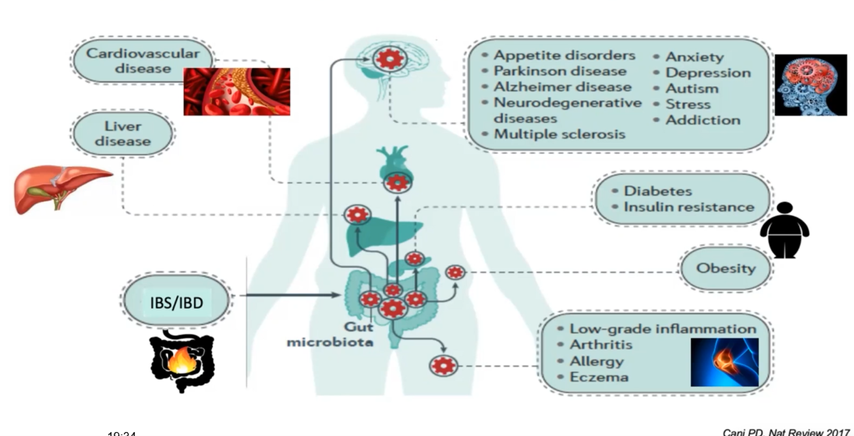
Dysbiose et pathologies chroniques
Un grand nombre de maladies chroniques ont un lien avec une altération du microbiote intestinal, notamment :
- Maladies cardiovasculaires;
- Maladies hépatiques comme la cirrhose;
- Maladies inflammatoires intestinales;
- Arthrites inflammatoires;
- Eczéma;
- Diabète et résistance à l’insuline;
- Sclérose en plaques;
- Obésité et troubles du comportement alimentaire;
- Maladies neurodégénératives comme Alzheimer et Parkinson;
- Troubles mentaux comme l’anxiété et la dépression;
- Autisme;
- Addictions.
Des signatures microbiennes
Certaines altérations du microbiote sont typiques de certaines maladies ou de certains états de santé. En effet, une étude a observé le microbiote intestinal de patients sains et malades (maladie de Crohn, fibromyalgie…) et a réussi, grâce à des analyses informatiques et à l’intelligence artificielle, à associer l’état de santé des patients en fonction de la composition de leur microbiote intestinal avec une fiabilité de 88%.
Dysbiose : cause ou conséquence ?
La plupart des études sur le sujet utilisent des modèles murins : des souris axéniques, sans microbiote, et des souris gnotobiotiques, avec un microbiote modifié. Après des manipulations de transfert de microbiotes, le comportement des différents groupes de souris est analysé. L’objectif ici est de montrer si le transfert d’un microbiote humain sur les souris peut également transmettre la maladie associée. C’est le cas dans la majorité des transferts.
Ainsi, l’altération du microbiote intestinal peut bien être la cause du développement de certaines pathologies comme l’obésité, la dépression ou la maladie de Crohn.
Comment préserver son microbiote ?
Comme vu précédemment, la résilience de notre microbiote est limitée et les altérations peuvent être irréversibles et conduire à une moins bonne santé, voire à des maladies.
De nombreux facteurs sont délétères à notre flore intestinale : stress, mauvaise alimentation, pollution, antibiotiques…
Il faut donc lutter contre l’appauvrissement de notre microbiote intestinal grâce à une alimentation saine, naturelle, riche en fibres (prébiotiques) et en aliments fermentés. Il est également important de ne pas avoir une hygiène excessive, surtout durant la petite enfance, et de maintenir une activité physique régulière tout au long de la vie. La prise de probiotiques peut aussi être une aide, notamment en cas de prise d’antibiotiques.
Questions/Réponses
Le jeûne a-t-il un impact positif ou négatif sur le microbiote intestinal ?
Déjà, il est important de distinguer les différents types de jeûne. La privation complète et prolongée de nourriture est déconseillée par la médecine de manière générale car, au-delà d’un impact incertain, voire négatif sur le microbiote intestinal, il peut y avoir de nombreux impacts négatifs sur le fonctionnement de notre organisme.
Comment peut-on connaître la composition de son microbiote intestinal ?
Des analyses coûtant de 200 à 300€ sont proposées par des entreprises privées. Il faut être prudent dans la mesure ou le but est très souvent de vendre des compléments alimentaires. Pour l’instant, les cliniciens ne sont de toute façon pas capables d’adapter leur prise en charge en fonction de la composition du microbiote intestinal du patient, cela répond donc à des questions de curiosité plutôt que de santé. Je pense néanmoins que d’ici 5-10 ans, des analyses de microbiotes mieux standardisées se démocratiseront et pourront être utiles à la prise en charge médicale.
Concernant l’amélioration du microbiote via un changement d’alimentation, j’ai l’impression que mon organisme s’habitue aux aliments facilitant le transit, si bien que l’effet bénéfique est limité au court terme malgré la persévérance de mes efforts. Comment l’expliquer ?
C’est très variable selon les individus. La prise de laxatifs doux sur le long terme tels que l’ispaghul est une solution envisageable pour réguler le transit intestinal. Il faut cependant vous rapprocher de votre médecin pour ce type de problématiques individuelles.
Que pensez-vous de la prise de probiotiques et d’acides gras à chaînes courtes comme le butyrate après l’arrêt des immunosuppresseurs suivant une greffe de moelle osseuse ?
Effectivement, comme après tout épisode durant lequel la flore intestinal a pu être altérée, cela peut être bénéfique pour la rééquilibrer. Tous les probiotiques ne sont pas équivalents et peu ont été testés scientifiquement. Encore une fois, il faut voir cela avec votre médecin pour être conseillé au mieux sur le type de probiotiques à prendre, car certains sont contre-indiqués dans des cas de port d’un cathéter central comme les ultra-levures qui peuvent coloniser le cathéter. Les probiotiques ont souvent une efficacité transitoire qui dure jusqu’à quelques semaines après leur arrêt, ce ne sont pas des microorganismes qui viennent s’implanter durablement dans le microbiote intestinal. Mais la prise régulière et prolongée de probiotiques peut être envisagée (toujours sur avis médical).
Que pensez-vous de la prise d’ultra levures concomitante avec un traitement antibiotique à vie comme l’amoxicilline ?
Je ne peux pas vous donner de réponses franches, mais les ultra-levures diminuent sûrement le risque de diarrhée, et ont probablement un impact bénéfique sur le microbiote intestinal.
Cette synthèse a été réalisée d’après la présentation de Dr Julien SCANZI. Visionnez le replay de cette conférence en cliquant sur ce lien.
Illustrations :
Références bibliographiques
- Yatsunenko, T., Rey, F., Manary, M. et al., Human gut microbiome viewed across age and geography. Nature 486,222–227 (2012).
- Dethlefsen, & D.A. Relman, Incomplete recovery and individualized responses of the human distal gut microbiota to repeated antibiotic perturbation, Proc. Natl. Acad. Sci. U.S.A. 108 (supplement_1) 4554-4561
- Lozupone, C., Stombaugh, J., Gordon, J. et al., Diversity, stability and resilience of the human gut microbiota. Nature 489,220–230 (2012).
- Falony G, Joossens M, Vieira-Silva S, Wang J, Darzi Y, Faust K, Kurilshikov A, Bonder MJ, Valles-Colomer M, Vandeputte D, Tito RY, Chaffron S, Rymenans L, Verspecht C, De Sutter L, Lima-Mendez G, D’hoe K, Jonckheere K, Homola D, Garcia R, Tigchelaar EF, Eeckhaudt L, Fu J, Henckaerts L, Zhernakova A, Wijmenga C, Raes J. Population-level analysis of gut microbiome variation. Science. 2016 Apr 29 ; 352(6285):560-4.
- Ianiro G, Tilg H, Gasbarrini A. Antibiotics as deep modulators of gut microbiota: between good and evil. Gut. 2016 Nov ; 65(11):1906-1915.
- Rothschild, D., Weissbrod, O., Barkan, E. et al., Environment dominates over host genetics in shaping human gut microbiota. Nature 555, 210–215 (2018).
- Minerbi A, Gonzalez E, Brereton NJB, Anjarkouchian A, Dewar K, Fitzcharles MA, Chevalier S, Shir Y., Altered microbiome composition in individuals with fibromyalgia. Pain. 2019 Nov ; 160(11):2589-2602.
- Vanessa K. Ridaura et al., Gut Microbiota from Twins Discordant for Obesity Modulate Metabolism in Mice. Science 341, 1241214 (2013).